Page 97 - Zmist-n5-2015
P. 97
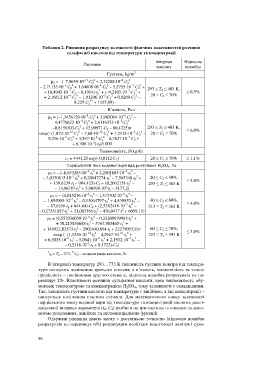
Таблиця 2. Рівняння розрахунку залежності фізичних властивостей розчинів
сульфатної кислоти від температури та концентрації
Інтервал Відносна
Рівняння
змінних похибка
3
Густина, kg/m
–8
6
–11
5
r 2 = –(–7,9659·10 ·С 2 + 2,32288·10 ·С 2 –
–6 4 –4 3 –3 2
– 2,71135·10 ·С 2 + 1,64608·10 ·С 2 – 5,5755·10 ·С 2 + 293 ≤ Т 2 ≤ 403 K,
5
–7
–2
*
+ 10,4943·10 ·С 2 – 0,1914)·t 2 + (–9,2103·10 ·С 2 + 20 ≤ С 2 ≤ 70% ≤ 0,5%
–4
4
–2
3
2
+ 2,16612·10 ·С 2 – 1,91206·10 ·С 2 + 0,8269·С 2 –
**
– 9,225·С 2 + 1127,89)
В’язкість, Pa·s
5
6
–8
–6
m 2 = (–1,3456129·10 ·С 2 + 3,902094·10 ·С 2 –
3
–4
–2
4
– 4,4770622·10 ·С 2 + 2,6116373·10 ·С 2 –
2
–0,8156303·С 2 + 12,99971·С 2 – 80,4225)´ 293 ≤ Т 2 ≤ 403 K, ≤ 6,0%
–12
–10
4
–7
5
6
´exp(–(1,822·10 ·С 2 – 7,68·10 ·С 2 + 1,2113·10 ·С 2 – 20 ≤ С 2 ≤ 70%
3
–6
–3
2
–4
– 9,216·10 ·С 2 + 3,587·10 ·С 2 – 6,7627·10 ·С 2 +
–2
+ 6,708·10 )·t 2 )/1000
Теплоємність, J/(kg·K)
с 2 = 4441,25·exp(–0,0112·С 2 ) 20 ≤ С 2 ≤ 70% ≤ 1,1%
Парціальний тиск водяної пари над розчинами Н 2 SO 4 , Pa
–5
–8
6
5
p 3 = – (–6,633285·10 ·t 2 + 2,2501685·10 ·t 2 –
–3
4
2
3
– 3,0330815·10 ·t 2 + 0,20847274·t 2 – 7,565348·t 2 + 20 ≤ С 2 < 40%, ≤ 5,0%
3
+ 139,8239·t 2 – 984,423)·C 2 + (0,2002151·t 2 – 293 ≤ Т 2 ≤ 363 K
2
2
– 13,96787·t 2 + 5,90498·10 ·t 2 – 5177,2)
–8
5
–5
6
p 3 = – (4,015276·10 ·t 2 – 1,373702·10 ·t 2 –
–3
2
4
3
– 1,894905·10 ·t 2 – 0,13044797·t 2 + 4,839852·t 2 – 40 ≤ С 2 < 60%, ≤ 4,0%
–3
4
– 87,6216·t 2 + 644,64)·C 2 + (2,5382418·10 ·t 2 – 313 ≤ Т 2 ≤ 363 K
2
3
2
– 0,27351657·t 2 + 21,063365·t 2 – 476,0477·t + 6059,15)
–4
6
5
p 3 = (8,557036059·10 ·t 2 – 0,33209839985·t 2 +
4
3
+ 50,215854648·t 2 – 3767,983445·t 2 +
2
+ 148922,83573·t 2 – 2903440,604·t 2 + 22279053,9)´ 60 ≤ С 2 ≤ 70%, ≤ 3,0%
6
5
–10
–12
´exp (–(1,1236·10 ·t 2 – 4,2967·10 ·t 2 + 323 ≤ Т 2 ≤ 393 K
–8
–4
–6
4
2
3
+ 6,5035·10 ·t 2 – 5,0641·10 ·t 2 + 2,1932·10 ·t 2 –
–2
– 0,5318·10 ·t 2 + 0,1722)·С 2 )
* **
t 2 = T 2 – 273, С 2 – концентрація кислоти, %.
В інтервалі температур 293…773 K залежність густини повітря від темпера-
тури описують поліномом третього степеня, а в’язкість, теплоємність та тепло-
провідність – поліномами другого степеня, відносна похибка розрахунків не пе-
ревищує 2%. Властивості розчинів сульфатної кислоти, крім теплоємності, обу-
мовлені температурою та концентрацією Н 2SO 4, тому залежності є складнішими.
Так, залежність густини кислоти від температури є лінійною, а від концентрації –
описується поліномом шостого степеня. Для математичного опису залежності
парціального тиску водяної пари від температури та концентрації кислоти, дослі-
джуваний інтервал параметрів (t 2, С 2) розбили на три частини та описали за допо-
могою поліномних, лінійних та експоненціальних функцій.
Одержані рівняння дають змогу з достатньою точністю (відносна похибка
розрахунків не перевищує 6%) розрахувати необхідні властивості повітря і суль-
96